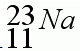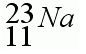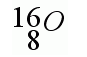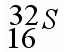УРОК 4
Тема: Будова атома
Мета:
- сформувати уявлення про будову атома і атомних ядер, ознайомити з поняттями «протони», «нейтрони», «електрони», «протонне» та «нейтронне числа»;
- розвивати вміння розраховувати кількість протонів та нейтронів у ядрах атомів, знаходити у ПС протонне та нуклонне числа для кожного елемента;
- виховувати науковий світогляд та інтерес до хімії.
Тип уроку: комбінований
Обладнання та матеріали: комп’ютер, інтерактивна дошка, презентація, періодична система хімічних елементів Д. І. Менделєєва, схема «Будова атома».
ХІД УРОКУ
|
Структура уроку |
Вид діяльності |
||||||||||||||||||||||||||||||||||||||||||||||||
|
І.Організація класу ІІ. Перевірка домашнього завдання Два учні біля дошки виконують домашнє письмове завдання. ІІІ. Актуалізація опорних знань 4 учні працюють на картках. Картка 1 1)Який елемент має найбільш виражені металічні властивості Магній чи Кальцій. 2) Що спільного між елементами головної та побічної підгруп? 3)Відносна молекулярна маса леткої сполуки з Гідрогеном елемента сьомої групи дорівнює 81.Що це за елемент? Картка 2 1)Який елемент має більш виражені неметалічні властивості Сульфур чи Селен? 2)Порівняйте малі та великі періоди ПСХЕ. 3)Відносна молекулярна маса вищого оксиду елемента ІV групи дорівнює 44. Назвіть цей елемент. Картка 3
Картка 4
Інші учні класу грають з вчителем в естафету: «Чарівна паличка»(Той, хто передає паличку задає запитання на тему: « Будова періодичної системи», - той, хто отримує - дає відповідь.) Аргументація оцінок за відповіді. IV. Мотивація навчальної діяльності Тему уроку сьогодні зашифровано в вірші Валерія Брюсова, відгадайте її. «… Быть может, каждый атом – Вселенная, где сто планет. Но также то, чего здесь нет».
V. Оголошення теми і постановка задач уроку Показ презентації(слайд1). VI. Вивчення нового матеріалу 1.Досліди Резерфорда Показ презентації(слайд2-5) 2. Поняття про атом Запис поняття з інтерактивної таблиці Атом –це найменша електронейтральна частинка, яка складається з позитивно зарядженого ядра і електронів, які рухаються навколо нього. 3. Будова атома Зображення опорної схеми разом з учнями, перевірка її правильності за інтерактивною дошкою(слайди 7,8). Собрать, сколько надо, частиц всех сортов, 4.Поняття та позначення протонного та уклонного числа Нуклонне число Протонне число← e- - електрони p+ - протони Z – порядковий номер елемента n0 - нейтрони A – нуклонне число A= Ar e- = p+= Z Ar - Z= n0 VII. Закріплення знань Гра « Країна самоцвітів» Кожен учень дістає зі скриньки самоцвіт з питанням і дає на нього відповідь, за яку отримує відповідну кількість балів. Картки для групової роботи. Картка №1 1. Запишіть «домашню адресу», тобто положення в періодичній системі Хімічного елемента Д. І. Менделєєва.
2. Визначте заряд ядра атома, загальну кількість електронів. 3. Визначте склад ядра атома. Картка №2 1. Запишіть «домашню адресу», тобто положення в періодичній системі Хімічного елемента Д. І. Менделєєва.
2. Визначте заряд ядра атома, загальну кількість електронів. 3. Визначте склад ядра атома. Картка №3 1. Запишіть «домашню адресу», тобто положення в періодичній системі Хімічного елемента Д. І. Менделєєва.
2. Визначте заряд ядра атома, загальну кількість електронів. 3. Визначте склад ядра атома. VIII. Домашнє завдання Опрацювати § 23, вивч конспект,ст..143 № 203 письмово Підготувати повідомлення про вплив радіоактивності на організм людини, ядерні реакції, атомні катастрофи. IX. Підведення підсумків уроку Он бежит по проводам, Очень положительный, Зарядом я похвастать не могу,
|
Перевірка письмового дом. завдання
Робота з картками
«Чарівна паличка»
Проблемне питання
Показ презентації з коментарем вчителя
Робота з Інтерактивною таблицею, складання конспекту
Проблемне питання
Складання опорного конспекту
Гра «Країна самоцвітів»
Групова робота за картками
Коментар вчителя
Загадки
|